《 酸和堿的中和反應(yīng)》教學(xué)設(shè)計(jì)
學(xué)習(xí)內(nèi)容: 課題二 酸和堿的中和反應(yīng)(第1課時(shí)) | 指導(dǎo)設(shè)計(jì) 教學(xué)反思 | 2、處理工廠的廢水 寫(xiě)出用熟石灰處理含硫酸的工廠污水時(shí)所發(fā)生反應(yīng)的化學(xué)方程式: 3、用于醫(yī)藥 用于治療胃酸過(guò)多的藥物中常含有Al(OH)3和 NaHCO3等物質(zhì),請(qǐng)寫(xiě)出胃酸(HCl)與這兩種成分反應(yīng)的化學(xué)方程式: 三、展示反饋: 有人說(shuō):凡是生成鹽和水的反應(yīng)就是中和反應(yīng),請(qǐng)問(wèn)對(duì)不對(duì)? 四、拓展延伸: (1)醋可以將熱水瓶膽壁上的水垢(主要成分是Mg(OH)2)除去,原理是什么。 (2)早晨空腹時(shí),為什么要少吃蘋(píng)果(或酸性食物)?涼胃后醫(yī)生建議吃的藥丸主要藥物應(yīng)該是酸性還是堿性?治療胃病的反應(yīng)原理是什么? 五、目標(biāo)檢測(cè): 1.向含有酚酞的NaOH溶液中,不斷滴入稀鹽酸。此過(guò)程燒杯中溶液顏色的變化是( ) A.由紅色變?yōu)樗{(lán)色 B.由藍(lán)色變?yōu)榧t色 C.由紅色變?yōu)闊o(wú)色 D.由無(wú)色變成紅色 2.下列應(yīng)用一定與中和反應(yīng)原理無(wú)關(guān)的是( ) A.施用熟石灰改良酸性土壤 B.服用含Al(OH)3的藥物治療胃酸過(guò)多 C.用熟石灰和硫酸銅配制波爾多液 D.用NaOH溶液洗滌石油產(chǎn)品中的殘余硫酸
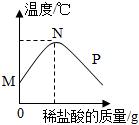
3.一定溫度下,向含有適量酚酞溶液的氫氧化鈉溶液中慢慢滴加稀鹽酸,溶液溫度隨加入稀鹽酸的質(zhì)量如圖所示。下列敘述正確的是( ) A.M點(diǎn)時(shí)溶液呈無(wú)色 B.N點(diǎn)時(shí)兩種溶液恰好完全反應(yīng) C.N點(diǎn)時(shí)溶液中含兩種溶質(zhì) D.P點(diǎn)時(shí),溶液中只含一種溶質(zhì) |
學(xué)習(xí)目標(biāo):1.知道酸和堿之間的中和反應(yīng),認(rèn)識(shí)反應(yīng)的實(shí)質(zhì); 2.了解中和反應(yīng)在生產(chǎn)、生活中的應(yīng)用,認(rèn)識(shí)化學(xué)對(duì)生產(chǎn)和改善人們生活質(zhì)量的重要性 | ||
重點(diǎn)、難點(diǎn):中和反應(yīng)的定義、實(shí)質(zhì)及其應(yīng)用。 | ||
一、 + 自主學(xué)習(xí): 自主學(xué)習(xí): 鹽:由金屬離子和酸根離子組成的化合物。 鹽=== 金屬離子(或NH4 ) + 酸根離子 舉例: 二、合作探究: 1.中和反應(yīng):?jiǎn)栴}:酸與堿之間會(huì)發(fā)生反應(yīng)嗎? 猜想:1、會(huì)反應(yīng) 2、不會(huì)反應(yīng) 實(shí)驗(yàn)方案:NaOH溶液中滴加無(wú)色酚酞(溶液變?yōu)榧t色)→逐滴加入HCl溶液并不斷攪拌→紅色變?yōu)闊o(wú)色。為什么隨著HCl溶液的加入,溶液的紅色會(huì)逐漸消失? 答:紅色消失是因?yàn)镹aOH溶液沒(méi)有了,與滴加的HCl溶液發(fā)生了化學(xué)反應(yīng)。 (1).酚酞在實(shí)驗(yàn)中起什么作用?_________________________ (2).為什么在操作中必須逐滴滴入稀鹽酸? 防止稀鹽酸滴加過(guò)量。 NaOH + HCl = NaCl +H2O
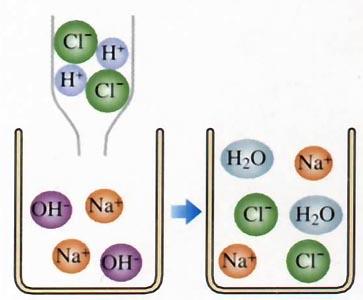
【歸納】 的反應(yīng),叫做中和反應(yīng)。中和反應(yīng)不是四大基本反應(yīng)類(lèi)型之一,前面我們學(xué)過(guò)的基本反應(yīng)類(lèi)型有哪些? 2.微觀實(shí)質(zhì): NaOH = Na+ + OH- HCl = Cl- + H+ NaOH + HCl = NaCl +H2O H+ + OH- = H2O 3.中和反應(yīng)的應(yīng)用 ①、改變土壤的酸堿性 酸性土壤中含有H2SO3,應(yīng)該用哪種物質(zhì)來(lái)改良該酸性土壤?寫(xiě)出相關(guān)化學(xué)方程式。 |
學(xué)生姓名: 年級(jí): 九 班級(jí): 科目:化學(xué) 學(xué)案類(lèi)別: 主備教師: 李云云 審核教師: 時(shí)間: 2021 年 3 月 日